新泽西理工学院(新泽西理工大学)研究人员公布了一项新技术使用液相色谱-光谱法(质)和电化学细胞(EC)流,他们说代表了怎样的“范式转换”制药实验室测试和产生新的蛋白质药物等治疗性单克隆抗体研制治疗各种各样的疾病,癌症和传染病。
研究人员说他们electrochemistry-based安全和质量测试方法可以让崭露头角的biotherapeutics要做一小部分由传统方法所需的时间,这通常需要漫长而昂贵的某些生物材料用于样品的生产测试。
新泽西理工大学开发的“这个方法我们有可能产生重大影响的定量蛋白质组学,它表示一个范式转换,即在制药工业的监测生物制药产品和过程质量控制杂质”,郝Chen说新泽西理工大学化学与环境科学系的教授。”,这项研究中,我们已经展示了一种可以量化的方法药物产品和工艺的杂质比已经可能更加迅速和准确。…我们希望它成为非常有用的促进治疗性蛋白和疫苗研发不同疾病的治疗和预防未来。”
传统测试,或蛋白质定量,需要耗时的制备合成isotope-labelled肽作为内部标准来衡量总蛋白浓度在sample-helping疗效和安全性的研究人员积极地监控治疗药物开发过程中蛋白质成分。为了克服这个限制,陈的实验室开发了一种电量质谱(CMS)蛋白质的绝对定量方法不使用标准。方法应用液相色谱-光谱法和电化学流动池快速量化和基于电化学检测目标蛋白或肽的变化特征。
“而不是等待周获得标准或试剂在传统的方法中,可以执行CMS定量实验。因此,它将有利于跟踪药物发现过程中杂质,确保其有效间隙与过程优化和控制”,陈先生说。
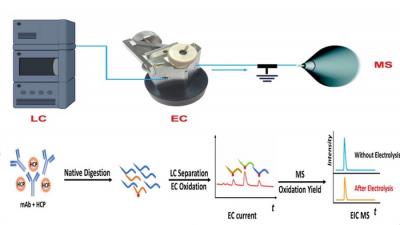
”这样一个装置允许我们单独的肽与液相色谱蛋白质消化后,监测肽的氧化电化学流动池产生电流和测量氧化率与质谱”,新泽西理工大学博士生永乐Ai解释道。”随着氧化电流信号的组合收益率为多肽和蛋白质的绝对定量提供了足够的信息。”
在他们的研究中,研究小组展示的CMS方法实现多个蛋白质的绝对定量(β-lactoglobulin B,α-lactalbumin和碳酸酐酶)的混合物在一个运行时,不使用任何标准。值得注意的是,该小组还展示了该方法的功能检测蛋白质deamidation-a常见治疗蛋白质降解事件产生的物理或化学强调整个生产过程和存储。
团队成功地量化几个蛋白质降解产物,包括蛋白质降解的关键中间体,琥珀酰亚胺的形成,也从来没有做过绝对量化由于缺乏标准,根据研究人员。
“缺乏标准是由在他们的挑战新创合成”,陈先生说。“能够准确地量化脱酰氨基作用的产品和中间体可以提供更好的理解治疗蛋白质降解,并有可能创建一个新的方法来研究疾病的病理和衰老的过程。”
现在,陈的实验室计划为大规模定量应用他们的新方法在一个运行数以千计的蛋白质。他们还计划提高他们CMS的敏感性分析允许量化复杂生物样品中蛋白质的含量非常低,这可能对研究成果,从临床诊断和药物研发精密医学鉴定和定量的样品在分子水平上是必要的。
“作为在生物蛋白质执行大量的功能,绝对的重要性蛋白质定量很难夸大”,陈表示。“CMS应该加快疾病诊断过程,药物发现和开发,现在打开一个新的门为生物学家和生物化学家探索大量的蛋白质在人体内可能提供重要的生物功能或角色为疾病生物标记物和药物靶标”。
新泽西理工大学团队的CMS方法的工作流程,结合液相色谱(LC),电化学氧化(EC)和质谱(MS)的定量测定蛋白质的丰度。信贷:新泽西理工大学












